#Purdon
Photo


Showy Lady’s Slipper
Cypripedium reginae
Orchidaceae
Photographs taken on June 18, 2023, at Purdon Conservation Area, Lanark Highlands, Ontario, Canada.
#wildflowers#wildflowers of southern ontario#Showy Lady’s Slipper#lady slipper#Cypripedium reginae#Cypripedium#Orchidaceae#orchid#pink#white#wildflower#flora#Purdon Conservation Area#Purdon#Lanark Highlands#Ontario#Canada
120 notes
·
View notes
Text
Where was POWASSAN Ontario? - A Lanark County Affiliation
Jamie Toeppner· Plenitudinous Powassan Photos page
July 1965 Scouts on canoe trip at Restoule Park
It seems that the folks from Lanark County not only did go West they went North too. There were many that went to Powassan from Lanark County and every two weeks The Lanark Era shared their social column. https://www.powassanlibrary.com/history-of-powassan
The Lanark Era
Lanark, Ontario,…

View On WordPress
#closs#genealogy#History#Immigration#Lanark-County#newpaper#north bay#ontario#POWASSAN#Purdon#social notes
0 notes
Text
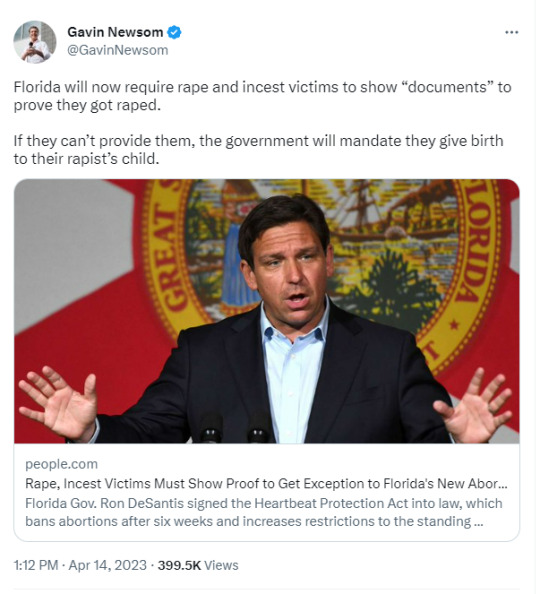
WHY IS THE PURDON OF PROOF FUCKING NECESSARY? ARE THE BRUISES NOT ENOUGH? GD THIS MAKES ME MAD-Yes this is in ALL CAPS because I am SCREAMING!
185 notes
·
View notes
Photo

Ribbon. late 19th–early 20th century. Credit line: Purchase, 1906 (through Sir Purdon Clark) https://www.metmuseum.org/art/collection/search/105151
#aesthetic#art#abstract art#art museum#art history#The Metropolitan Museum of Art#museum#museum photography#museum aesthetic#dark academia
7 notes
·
View notes
Text
Interesting Papers for Week 9, 2024
Species-specific wiring of cortical circuits for small-world networks in the primary visual cortex. Baek, S., Park, Y., & Paik, S.-B. (2023). PLOS Computational Biology, 19(8), e1011343.
Value dynamics affect choice preparation during decision-making. Balewski, Z. Z., Elston, T. W., Knudsen, E. B., & Wallis, J. D. (2023). Nature Neuroscience, 26(9), 1575–1583.
Concurrent Implicit Adaptation to Multiple Opposite Perturbations. Bernier, P.-M., Puygrenier, A., & Danion, F. R. (2023). ENeuro, 10(8).
Enhancing reinforcement learning models by including direct and indirect pathways improves performance on striatal dependent tasks. Blackwell, K. T., & Doya, K. (2023). PLOS Computational Biology, 19(8), e1011385.
Prominent in vivo influence of single interneurons in the developing barrel cortex. Bollmann, Y., Modol, L., Tressard, T., Vorobyev, A., Dard, R., Brustlein, S., … Cossart, R. (2023). Nature Neuroscience, 26(9), 1555–1565.
Extensive topographic remapping and functional sharpening in the adult rat visual pathway upon first visual experience. Carvalho, J., Fernandes, F. F., & Shemesh, N. (2023). PLOS Biology, 21(8), e3002229.
Psychophysiological stress influences temporal accuracy. Cellini, N., Grondin, S., Stablum, F., Sarlo, M., & Mioni, G. (2023). Experimental Brain Research, 241(9), 2229–2240.
Synaptic weights that correlate with presynaptic selectivity increase decoding performance. Gallinaro, J. V., Scholl, B., & Clopath, C. (2023). PLOS Computational Biology, 19(8), e1011362.
Efficient sampling-based Bayesian Active Learning for synaptic characterization. Gontier, C., Surace, S. C., Delvendahl, I., Müller, M., & Pfister, J.-P. (2023). PLOS Computational Biology, 19(8), e1011342.
Investigating the ability of astrocytes to drive neural network synchrony. Handy, G., & Borisyuk, A. (2023). PLOS Computational Biology, 19(8), e1011290.
Switching state-space modeling of neural signal dynamics. He, M., Das, P., Hotan, G., & Purdon, P. L. (2023). PLOS Computational Biology, 19(8), e1011395.
Receptive field sizes and neuronal encoding bandwidth are constrained by axonal conduction delays. Hladnik, T. C., & Grewe, J. (2023). PLOS Computational Biology, 19(8), e1010871.
A principal odor map unifies diverse tasks in olfactory perception. Lee, B. K., Mayhew, E. J., Sanchez-Lengeling, B., Wei, J. N., Qian, W. W., Little, K. A., … Wiltschko, A. B. (2023). Science, 381(6661), 999–1006.
Estradiol Receptors Inhibit Long-Term Potentiation in the Dorsomedial Striatum. Lewitus, V. J., & Blackwell, K. T. (2023). ENeuro, 10(8).
Functional and spatial rewiring principles jointly regulate context-sensitive computation. Li, J., Rentzeperis, I., & van Leeuwen, C. (2023). PLOS Computational Biology, 19(8), e1011325.
Rapid memory encoding in a recurrent network model with behavioral time scale synaptic plasticity. Li, P. Y., & Roxin, A. (2023). PLOS Computational Biology, 19(8), e1011139.
A triple distinction of cerebellar function for oculomotor learning and fatigue compensation. Masselink, J., Cheviet, A., Froment-Tilikete, C., Pélisson, D., & Lappe, M. (2023). PLOS Computational Biology, 19(8), e1011322.
Intrinsic motivation for choice varies with individual risk attitudes and the controllability of the environment. Munuera, J., Ribes Agost, M., Bendetowicz, D., Kerebel, A., Chambon, V., & Lau, B. (2023). PLOS Computational Biology, 19(8), e1010551.
Hybrid predictive coding: Inferring, fast and slow. Tscshantz, A., Millidge, B., Seth, A. K., & Buckley, C. L. (2023). PLOS Computational Biology, 19(8), e1011280.
Auditory cortex ensembles jointly encode sound and locomotion speed to support sound perception during movement. Vivaldo, C. A., Lee, J., Shorkey, M., Keerthy, A., & Rothschild, G. (2023). PLOS Biology, 21(8), e3002277.
#neuroscience#science#research#brain science#scientific publications#cognitive science#neurobiology#cognition#psychophysics#neurons#neural computation#neural networks#computational neuroscience
8 notes
·
View notes
Text

supanovaexpo: There were loads of laughs to be had today with Supa-Stars @wildpip_morley and @elizajaneface! 📸 Maddie Purdon
41 notes
·
View notes
Text
This is a post about a grave matter
5 notes
·
View notes
Photo



Purdon Conservation Area and Its Showy Lady Slipper Orchids
Photographs taken on June 18, 2023, at Purdon Conservation Area, Lanark Highlands, Ontario, Canada.
#wildflowers of southern ontario#Purdon Conservation Area#Purdon#Showy Lady Slipper Orchids#lady slipper orchid#Showy Lady Slipper Orchid#orchid#lady slipper#white#Lanark Highlands#ontario#canada#wildflowers#wildflower#flowers#flower#flora#nature#conservation area
44 notes
·
View notes
Text
Documenting Gladys Purdon Hart McDonald's Corners-- The Poland Baseball Team
Stuart McIntosh
Alexander Watt taught at Hart’s school on the corner on the corner of the East Half of lot 25, Con. 3 about 1 mile from his home in Lammermoor for half a day and then walked about 3 miles across country to teach at the Poland School the other half of the day. This would have taken place prior to 1830 as the School Act of 1827 required teachers to have certain qualifications. He…

View On WordPress
#author#genealogy#Gladys Purdon Hart#Hart#History#Lanark-County#mcdonalds&039;s corners#ontario#Poland Baseball Team#Purdon#writing
0 notes
Photo










This is a showy lady slipper orchid colony blog until further notice.
Purdon Conservation Area, Lanark, Ontario
June 19, 2022
11 notes
·
View notes
Photo

Cada 22 de julio se rinde homenaje a aquellos pacientes que padecen de una enfermedad causada por la mutación de un gen vinculado al cromosoma X. Se celebra el Día Mundial del Síndrome del Cromosoma X Frágil.
Con la celebración de esta efeméride se pretende divulgar información acerca de esta patología, así como promover la inclusión de las personas diagnosticadas con este síndrome.
¿Qué es el Síndrome del Cromosoma X Frágil?
El Síndrome del Cromosoma X Frágil, también conocido como el Síndrome Martin-Bell, es un trastorno genético caracterizado por la mutación del gen FMR1, asociado al cromosoma X. Este gen produce una proteína necesaria para que el cerebro crezca adecuadamente.
En 1943 los científicos James Purdon. Martin y Julia Bell descubrieron rasgos peculiares en pacientes que padecían algún retraso hereditario, asociado al cromosoma X que se vincula con la discapacidad cognitiva. Posteriormente, en 1991 el científico Lubs descubrió el gen vinculado a la enfermedad.
Esta patología se presenta en ambos sexos, con menor prevalencia en el sexo femenino, ya que poseen dos cromosomas X, siendo protegidas por el segundo cromosoma.
Algunos de los síntomas o características de este síndrome son los siguientes, asociados al comportamiento y rasgos físicos:
Discapacidad intelectual.
Retraso en el habla y el lenguaje.
Tendencia a evitar el contacto visual.
Dificultades para gatear, caminar o voltearse.
Palmotear o morderse las manos.
Comportamiento hiperactivo o impulsivo.
Articulaciones flexibles y tono muscular bajo.
Pies planos.
Piel suave.
Aumento de las dimensiones del cuerpo, orejas o frente.
Mandíbula prominente.
Cara alargada.
Tales rasgos característicos se presentan en los primeros meses de vida del paciente o después de la pubertad.
Comparte información útil e interesante sobre el Día Mundial del Síndrome del Cromosoma X Frágil en las redes sociales. Utiliza los hashtags #SíndromeXFrágil #DíaMundialdelSíndromeXFrágil
3 notes
·
View notes
Photo

Ribbon. 19th century. Credit line: Purchase, 1906 (through Sir Purdon Clark) https://www.metmuseum.org/art/collection/search/79090
#aesthetic#art#abstract art#art museum#art history#The Metropolitan Museum of Art#museum#museum photography#museum aesthetic#dark academia
6 notes
·
View notes



